Diabetes melitus tipe 2 (DM tipe 2) telah menjadi salah satu masalah kesehatan masyarakat paling serius di dunia. DM tipe 2 ditandai dengan resistensi insulin, disfungsi sel β, dan hiperglikemia kronik yang menyebabkan komplikasi multiorgan. Terapi konvensional terutama menargetkan pengendalian glikemik, namun seringkali gagal mencegah cedera pankreas dan hati yang progresif. Secretome yang berasal dari mesenchymal stem cell (MSC) telah menunjukkan dapat memodulasi respons imun, mengurangi peradangan, meningkatkan perbaikan jaringan, dan meningkatkan sensitivitas insulin. Hasil suatu penelitian pada hewan telah menunjukkan bahwa pengobatan dengan MSC-secretome hipoksik secara efektif memperbaiki resistensi insulin serta mengurangi kerusakan hati dan pankreas pada tikus DM tipe 2, sehingga berpotensi sebagai strategi terapi non-sel baru untuk gangguan metabolisme seperti DM tipe 2.
Diabetes melitus tipe 2 (DM tipe 2) telah menjadi salah satu masalah kesehatan masyarakat paling serius di dunia. International Diabetes Federation (IDF) memperkirakan bahwa lebih dari 537 juta orang (berusia 20-79 tahun) di seluruh dunia saat ini hidup dengan diabetes, dan angka ini diproyeksikan akan terus meningkat hingga mencapai sekitar 783 juta pada tahun 2045. DM tipe 2 ditandai dengan resistensi insulin, disfungsi sel β, dan hiperglikemia kronik yang menyebabkan komplikasi multiorgan. Terapi konvensional terutama menargetkan pengendalian glikemik, namun seringkali gagal mencegah cedera pankreas dan hati yang progresif.
Berbeda dengan terapi konvensional, secretome yang berasal dari mesenchymal stem cell (MSC) telah menunjukkan dapat memodulasi respons imun, mengurangi peradangan, meningkatkan perbaikan jaringan, dan meningkatkan sensitivitas insulin, sehingga menawarkan pendekatan terapeutik yang menjanjikan untuk mencegah atau mengurangi komplikasi terkait DM tipe 2, termasuk kerusakan hati dan pankreas.
Hasil suatu penelitian pada hewan telah menunjukkan bahwa secretome dari adipose MSC dapat mengurangi hiperglikemia dengan meningkatkan regenerasi sel-beta dan menurunkan resistensi insulin pada tikus dengan DM tipe 2.
Penelitian lebih lanjut juga telah dilakukan untuk menyelidiki potensi terapeutik secretome dari MSC hipoksik dalam memperbaiki resistensi insulin dan memulihkan integritas jaringan pada model tikus DM tipe 2. Dalam penelitian ini, tikus Wistar jantan diinduksi DM tipe 2 menggunakan diet tinggi lemak diikuti dengan pemberian streptozotocin–nicotinamide dan kemudian diobati dengan MSC-secretome secara intraperitoneal selama empat minggu. Kadar insulin serum dan indeks Homeostasis Model Assessment of Insulin Resistance (HOMA-IR) dinilai, diikuti dengan evaluasi histologi jaringan hati dan pankreas.
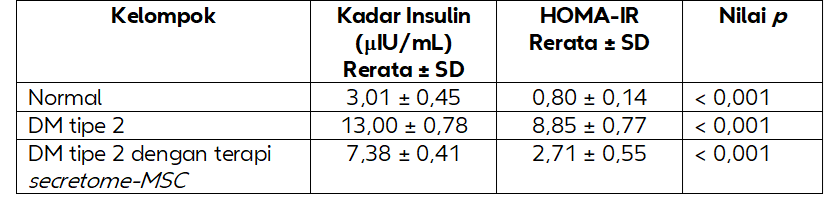
Hasil penelitian menunjukkan bahwa DM tipe 2 secara signifikan berhubungan dengan peningkatan kadar insulin dan nilai HOMA-IR dibandingkan dengan kelompok normal, hal ini mengonfirmasi adanya resistensi insulin. Pengobatan dengan MSC-secretome secara signifikan mengurangi kedua parameter tersebut (p < 0,001), yang menunjukkan peningkatan sensitivitas insulin. Analisis histologi menunjukkan degenerasi hati dan pankreas yang substansial pada tikus diabetes yang tidak diobati, ditandai dengan vakuolisasi hepatoseluler, steatosis, dan nekrosis pulau Langerhans. Pengobatan MSC-secretome menunjukkan pemulihan arsitektur lobular yang baik, penurunan akumulasi lipid, dan regenerasi pulau Langerhans pankreas. Efek perbaikan ini dikaitkan dengan komponen bioaktif secretome yang meregulasi stres oksidatif, peradangan, dan regenerasi sel.
Kesimpulan:
Pengobatan dengan MSC-secretome hipoksik secara efektif memperbaiki resistensi insulin serta mengurangi kerusakan hati dan pankreas pada tikus DM tipe 2, sehingga berpotensi sebagai strategi terapi non-sel baru untuk gangguan metabolisme seperti DM tipe 2.
Gambar: Ilustrasi (Sumber: Envato elements Gen AI)
Referensi:
- Wulandari PKA, Sari FN, Ardianto O, Widyatmoko A. Therapeutic role of MSC-secretome in type 2 diabetic models: correlation between improved HOMA-IR and attenuated pancreatic-hepatic structural alterations. International Journal of Cell and Biomedical Science 2025;4(10):339-48.
- Miklosz A, Chabowski A. Adipose-derived mesenchymal stem cells therapy as a new treatment option for diabetes mellitus. J Clin Endocrinol Metab. 2023;108(8):1889–197. doi:10.1210/clinem/dgad142