Ranitidine yang diproduksi oleh PT. Kalbe Farma Tbk., dan PT. Hexpharm Jaya, berdasarkan Surat dari BPOM dengan nomor: T-PW.03.02.3.351.11.19.4454, tertanggal 20 November 2019, yang ditandatangani
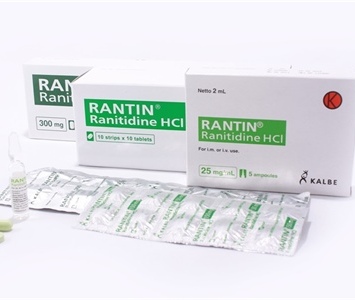
Ranitidine yang diproduksi oleh PT. Kalbe Farma Tbk., dan PT. Hexpharm Jaya, berdasarkan Surat dari BPOM dengan nomor: T-PW.03.02.3.351.11.19.4454, tertanggal 20 November 2019, yang ditandatangani oleh Deputi Bidang Pengawasan Obat, Narkotika, Psikotropika, Prekursor dan Zat Adiktif, diperbolehkan untuk dipasarkan kembali di seluruh wilayah Republik Indonesia.
Sebelumnya, Badan POM telah menerbitkan Informasi Awal untuk Tenaga Profesional Kesehatan pada tanggal 17 September 2019 terkait Keamanan Produk Ranitidin yang terkontaminasi NDMA. Badan POM memerintahkan kepada Industri Farmasi pemegang izin edar produk tersebut untuk melakukan penghentian produksi dan distribusi, dan melakukan pengambilan dan pengujian beberapa sampel produk ranitidin. Hasil uji sebagian sampel mengandung cemaran NDMA dengan jumlah yang melebihi batas yang diperbolehkan. Pengujian dan kajian risiko akan dilanjutkan terhadap seluruh produk yang mengandung ranitidin., hal ini sehubungan adanya kasus cemaran NMDA (N-Nitrosodimethylamine) yang disinyalir mempunyai potensi sebagai bahan karsinogenik disampaikan oleh US Food and Drug Administration (US FDA) dan European Medicine Agency (EMA).
Silahkan baca juga: Rantin, ranitidine untuk mengatasi produksi asam lambung berlebihan
Dengan adanya surat resmi dari BPOM ini menunjukkan bahwa produk ranitidine dari PT. Kalbe Farma Tbk., dan PT. Hexpharm Jaya dapat digunakan dan dikonsumsi kembali dengan aman. (Red)